Electrocoagulación en tratamiento de aguas residuales: mecanismo, ventajas y aplicaciones
La electrocoagulación es un proceso electroquímico innovador utilizado para remover contaminantes presentes en las aguas residuales. Mediante la disolución controlada de un ánodo metálico —generalmente de hierro o aluminio— se generan iones que desestabilizan partículas coloidales y emulsiones, facilitando su separación mediante procesos convencionales de decantación o flotación.
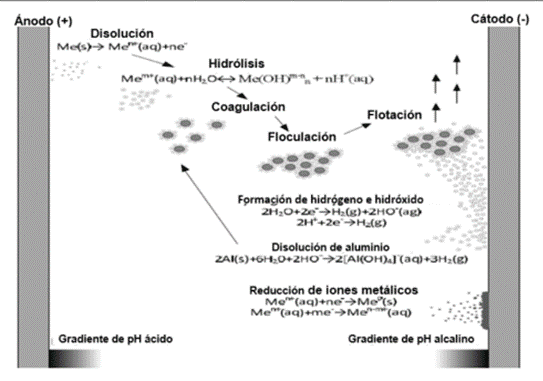
Mecanismo de reacción de la electrocoagulación
Durante la electrólisis, ocurren simultáneamente reacciones físicas y químicas que permiten la remoción de contaminantes.
Reacciones principales
-
En el ánodo (oxidación): se liberan iones metálicos (Fe³⁺ o Al³⁺), que actúan como coagulantes.
-
En el cátodo (reducción): se generan burbujas de hidrógeno que favorecen la flotación de partículas.
-
Los iones metálicos neutralizan las cargas eléctricas de los coloides, provocando su aglomeración en flóculos que pueden separarse por sedimentación o flotación.
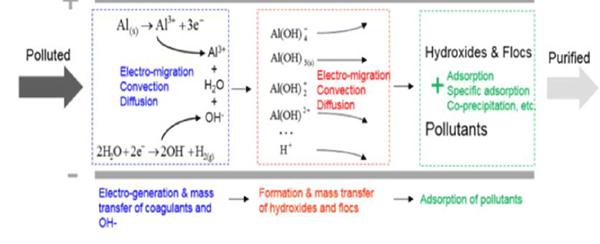
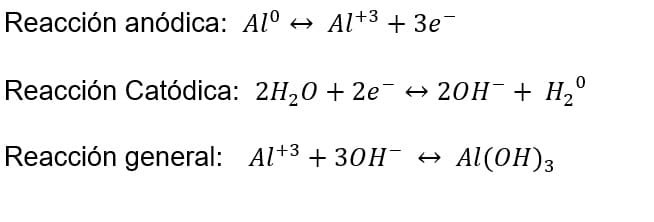
Factores que influyen en la eficiencia del proceso
-
pH: influye en la solubilidad del metal y en la formación de hidróxidos metálicos.
-
Densidad de corriente: a mayor densidad, se incrementa la remoción y el consumo energético.
-
Configuración del reactor: define la eficiencia de transferencia iónica.
-
Diseño del rectificador: controla la estabilidad del voltaje aplicado.
-
Tipo de reactor: determina el tiempo de contacto y la homogeneidad del proceso.
Tipos de reactores y celdas electrolíticas
- Tipos de reactores
El reactor Batch es el más adecuado para la electrocoagulación en aguas residuales industriales. Consiste en una celda con varios electrodos conectados a una fuente de poder, sumergidos en un volumen fijo de agua. Opera con caudal constante, bajo costo y fácil manejo. Su eficiencia depende del área superficial de los electrodos, ya que una mayor superficie favorece la disolución de iones y la remoción de contaminantes. La temperatura óptima de operación es de 60 °C.

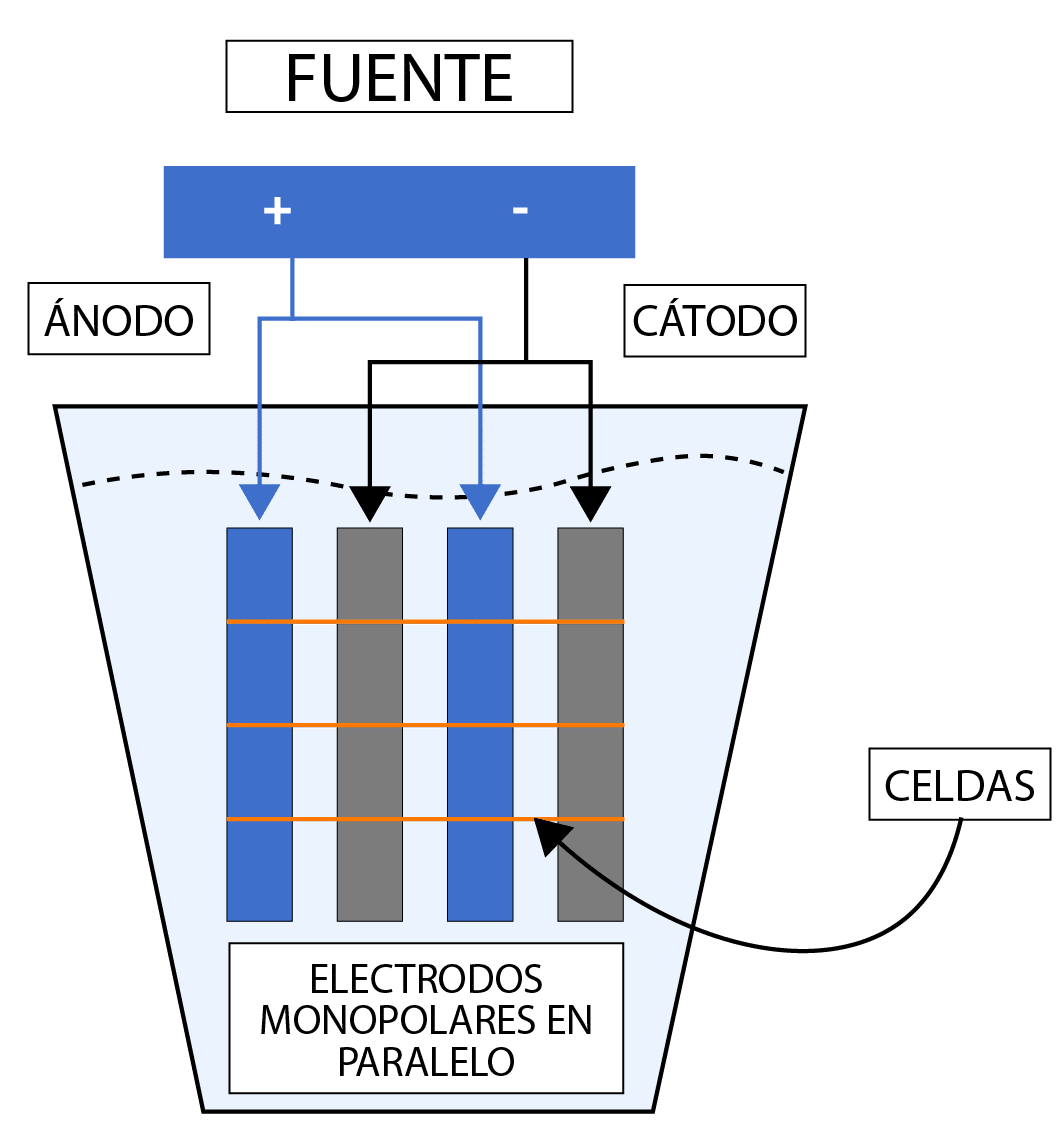

Comparación: coagulación convencional vs. electrocoagulación
| Aspecto | Coagulación química | Electrocoagulación (EC) |
|---|---|---|
| Fuente del coagulante | Sales metálicas externas (FeCl₃, Al₂(SO₄)₃) | Generado in situ por disolución anódica |
| Reactivos químicos | Requiere dosificación manual | No requiere coagulantes añadidos |
| Lodos generados | Mayor volumen, difícil manejo | Menor volumen y mayor estabilidad |
| Costos operativos | Elevados por reactivos | Reducción significativa de OPEX |
| Automatización | Limitada | Alta integración con control electrónico |
A diferencia de la coagulación tradicional, la electrocoagulación genera el agente coagulante in situ, reduciendo el consumo químico y la generación de residuos. Sin embargo, requiere reemplazo periódico del ánodo, control de conductividad mínima (aguas con STD > 200 μS/cm) y limpieza para evitar la formación de óxidos en el cátodo.
Limitaciones y consideraciones operativas
-
Requiere agua con conductividad suficiente para permitir el paso de corriente.
-
Formación de película de óxido en el cátodo, mitigable mediante inversión de polaridad.
-
Lodos ricos en hierro o aluminio, según el electrodo usado.
-
Necesidad de rectificadores de corriente estables para optimizar el rendimiento.
-
Requiere un mantenimiento programado de electrodos para evitar pérdida de eficiencia.
Casos de sistema de electrocoagulación a nivel piloto en sector curtiduría en Perú
La electrocoagulación es una tecnología que puede aplicar en aguas superficiales y subterráneas como en aguas residuales industriales y urbanas.
En las últimas décadas se ha utilizada para diferentes usos: tratamiento de aguas residuales industriales conteniendo metales pesados, industria de procesado de metales, minería e industrias papelera, residuos alimentarios, eliminación de aceites, eliminación de partículas suspendidas, materia orgánica de lecherías, defluoración del agua, tinturas y colorantes, aguas residuales con detergentes sintéticos, soluciones conteniendo metales pesados, amoníaco, entre otros.
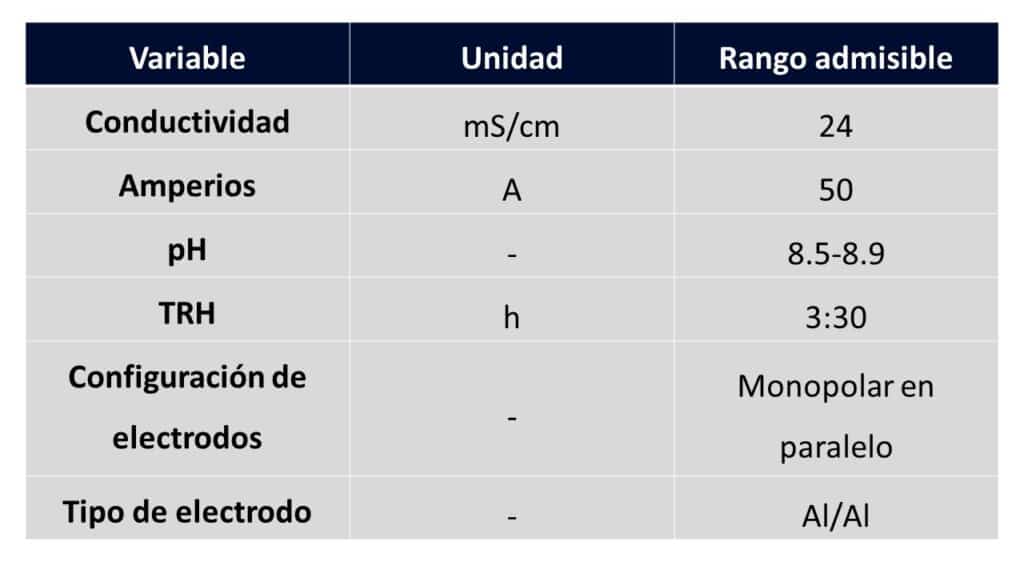
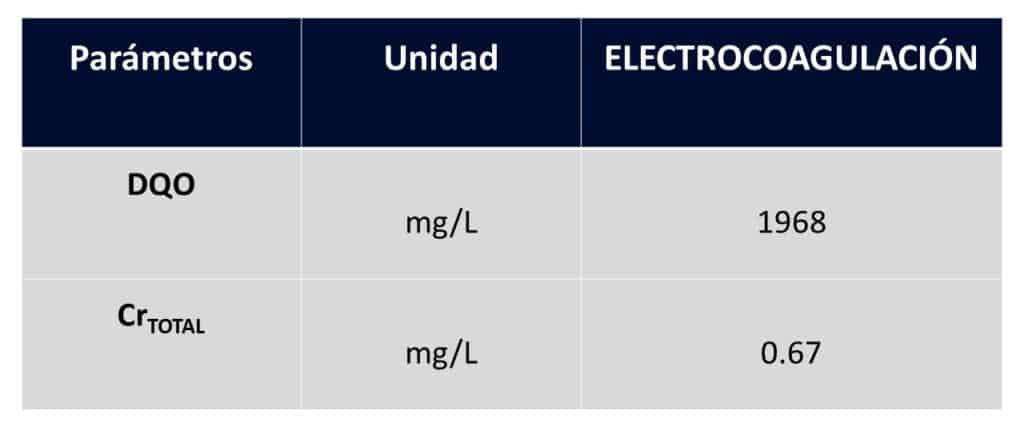
CASO 1: Curtiembre 1
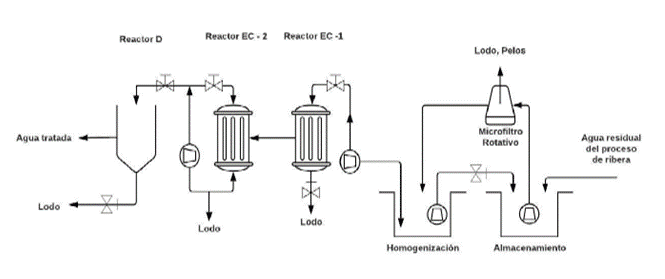
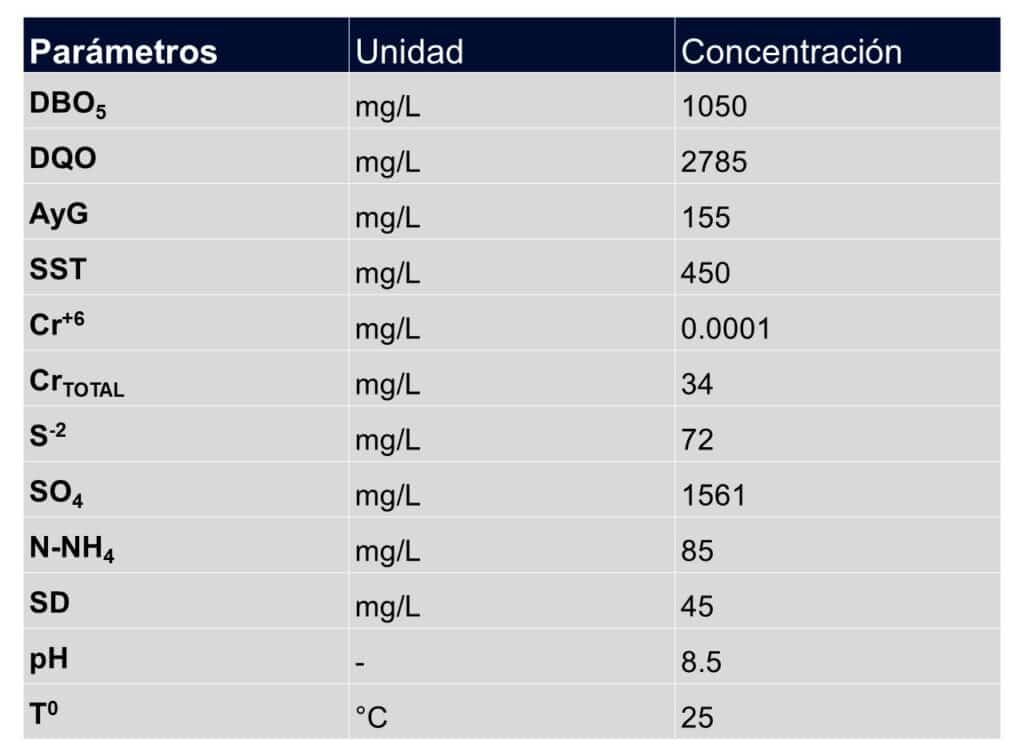
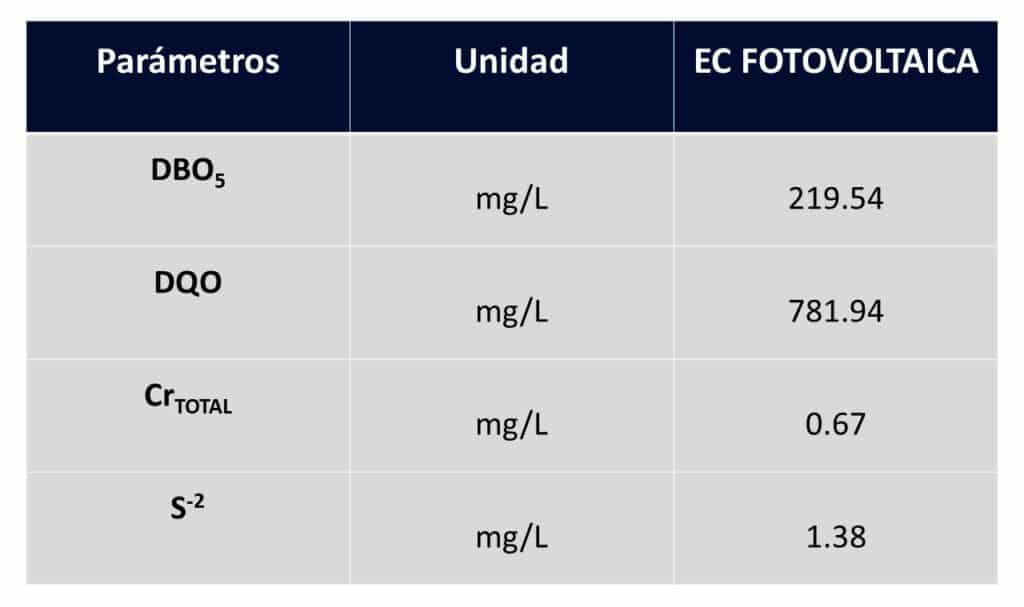
CASO 2: Curtiembre 2
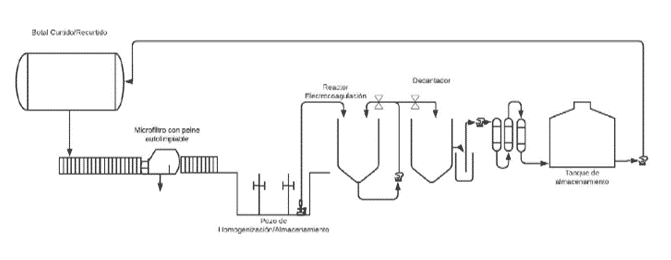
📘 Referencia externa:
Consulta los Límites Máximos Permisibles (DS 010-2010-MINAM)




