Eliminación de metales pesados en efluentes mineros: métodos y consideraciones
En zonas altoandinas con actividad minera, uno de los retos más críticos es la eliminación de metales pesados en efluentes mineros y metalúrgicos. A continuación, revisamos las técnicas más utilizadas, criterios de diseño, ventajas y limitaciones para seleccionar el tren de tratamiento adecuado.
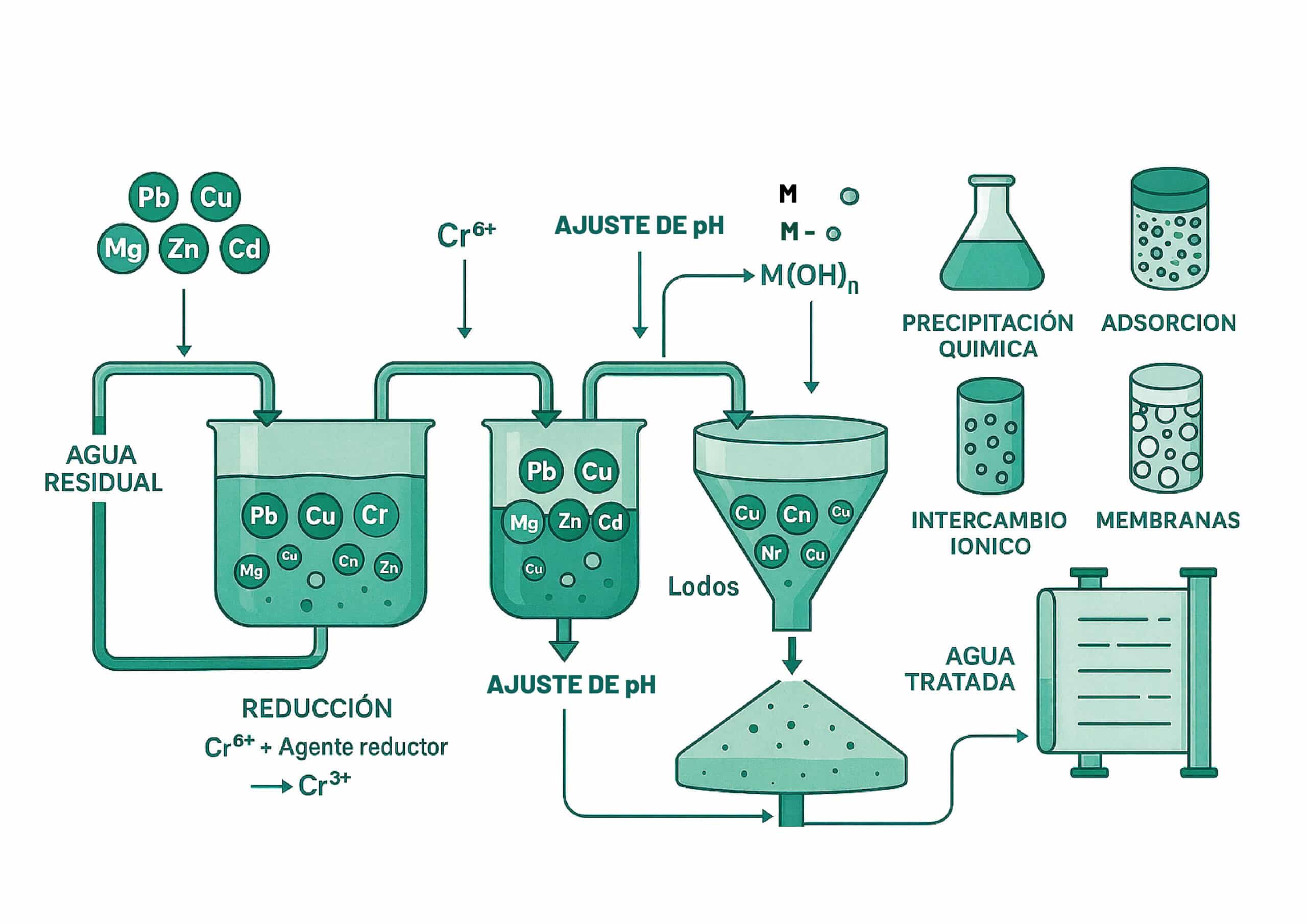
1) Precipitación con cal (hidróxidos)
La cal viva (CaO) y la cal hidratada (Ca(OH)₂) se emplean formando lechada de cal. Al dosificarla, el OH⁻ reacciona con los metales para formar hidróxidos metálicos insolubles (por ejemplo, Fe(OH)₃, Cu(OH)₂), que luego se separan por sedimentación o flotación.
Claves técnicas:
-
La cal es poco soluble; se trabaja como lechada preparada en tanques dedicados.
-
En efluentes ácidos con sulfatos, puede formarse yeso (CaSO₄); solo precipita en concentraciones elevadas.
-
Desventaja: genera alto volumen de lodos (impacta OPEX por disposición).
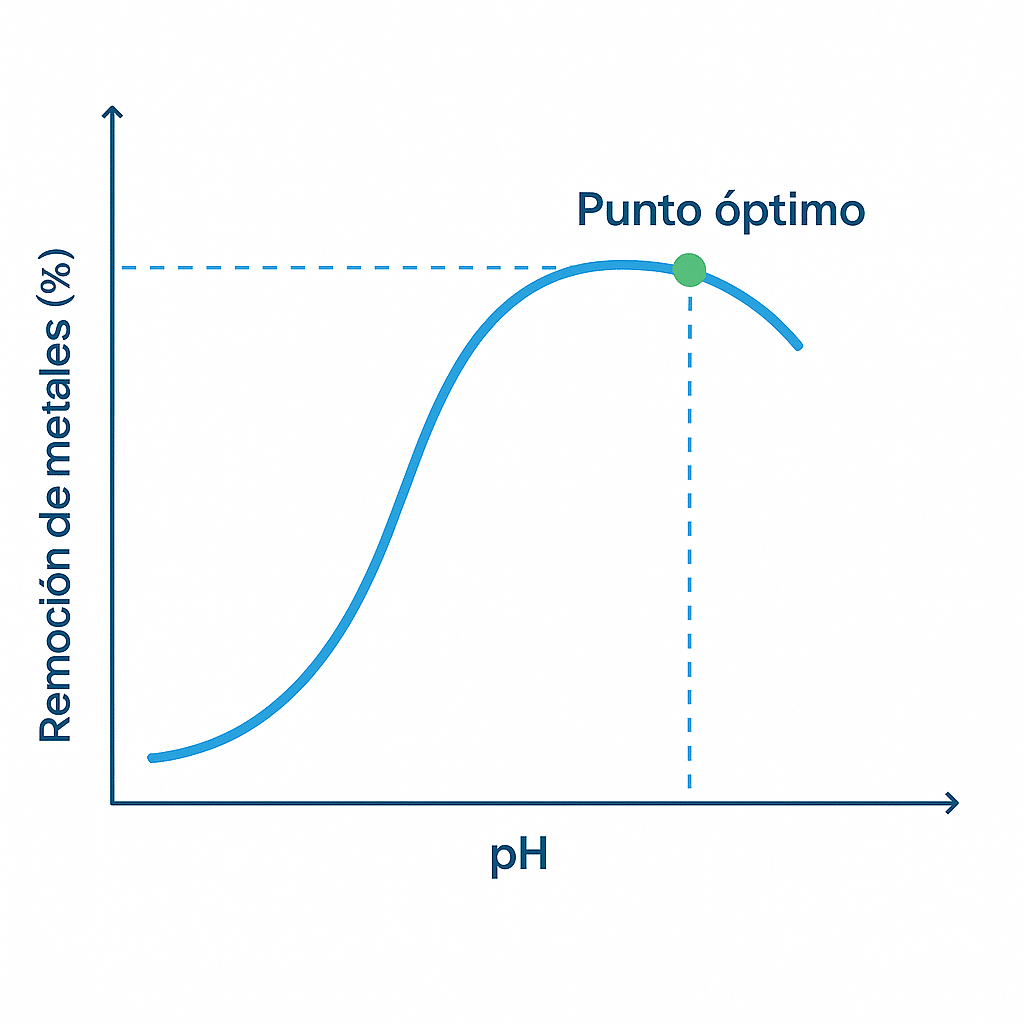
2) Curva de titulación (pH–dosis)
La curva de titulación define la dosis/pH óptimos de cal (u otra base). Es dependiente del agua real.
Ejemplo: al pasar de 1 a 2 mL de dosificante, el pH puede saltar de 2.71 a 11.3; por ello, pilotear evita sobreconsumos y sobrerreacciones.
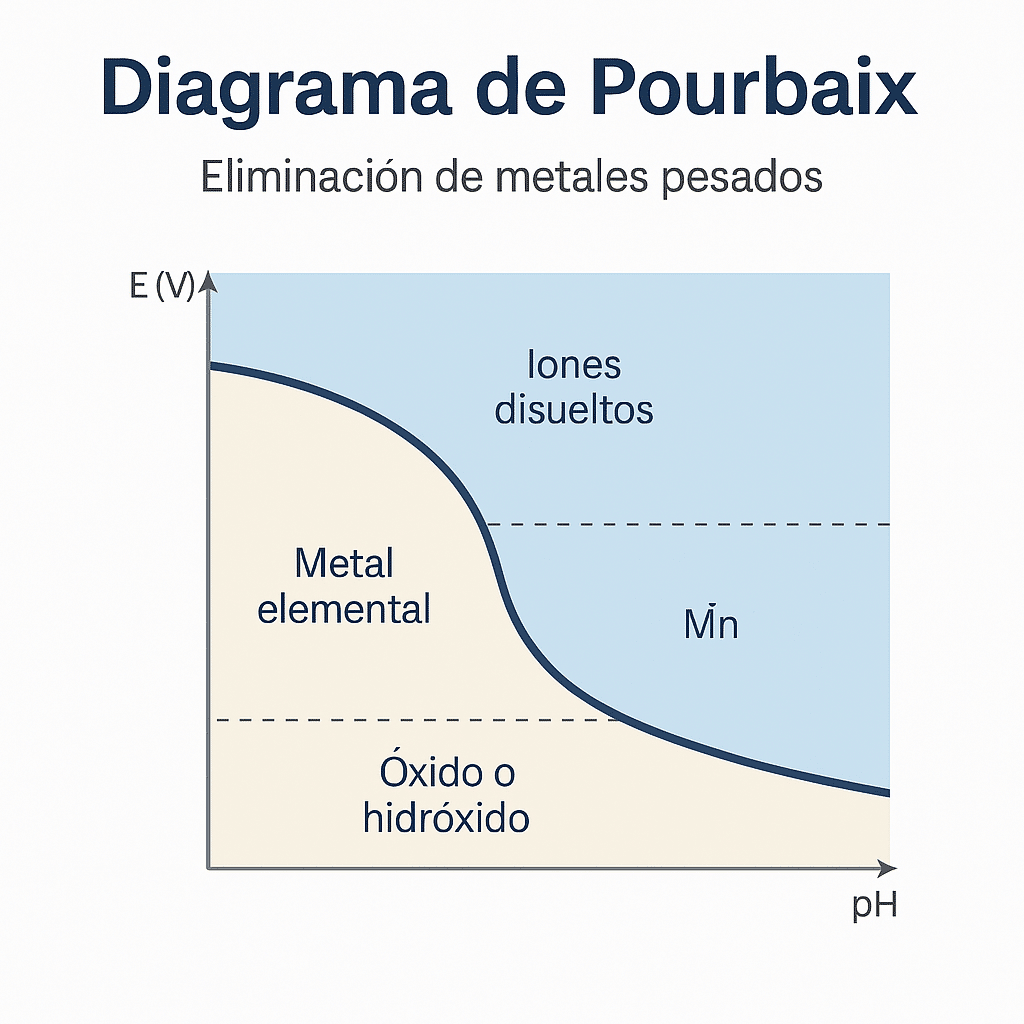
3) Diagrama de Pourbaix (pH–ORP)
El diagrama de Pourbaix ayuda a prever en qué zona (disolución, corrosión o pasivación) se encuentra un metal según su pH y ORP.
-
Ej.: a pH 3 y ORP bajo, el plomo puede estar como Pb²⁺.
-
Elevando a pH 8.5–9 precipita Pb(OH)₂/Pb(OH)₃; con ORP alto puede formarse PbO₂.
-
Ajustar pH y/o ORP (con oxidantes) permite mover el equilibrio hacia especies precipitables.
4) Coloración por estado de oxidación
Cada metal y estado de oxidación tiene una coloración característica (útil como indicador cualitativo). Aun así, la confirmación debe hacerse por análisis (por ejemplo, ICP, AAS).

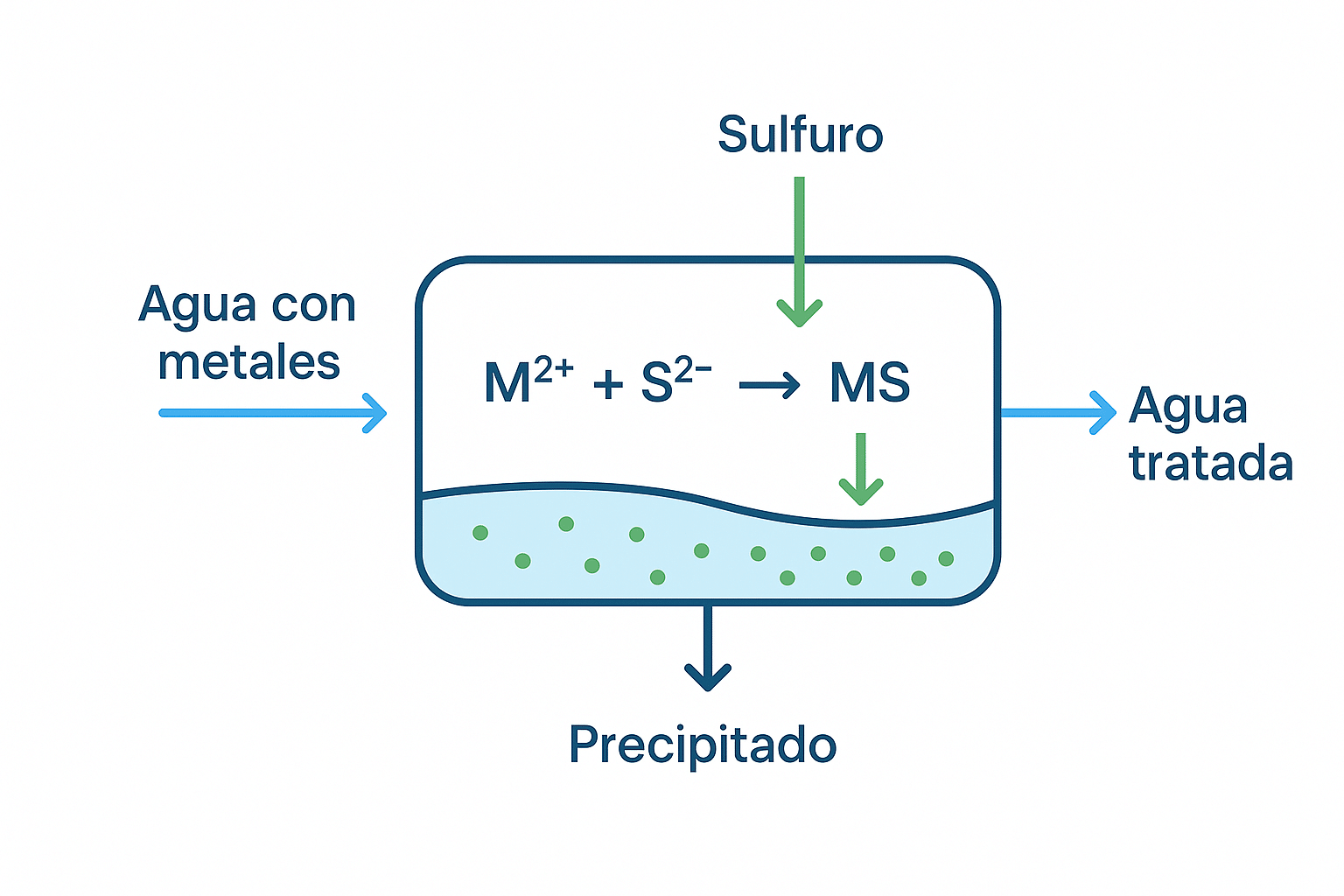
5) Precipitación con sulfuros
La reacción metal + sulfuro → sulfuro metálico (p.ej., CuS, ZnS) logra bajas solubilidades y menor generación de lodos que con cal.
Ventajas
-
Puede operar a pH moderado (6–8), reduciendo consumo de base y sales.
-
Lodos más densos y con menor volumen.
Consideraciones
-
Requiere control de ORP (el azufre es reductor).
-
Manejo seguro de sulfuros por toxicidad y olor (H₂S).
-
Sistemas cerrados y ventilación controlada reducen riesgos.
6) Oxidación para favorecer la eliminación
La oxidación (con H₂O₂, O₃, Cl₂, etc.) eleva el ORP y facilita la formación de óxidos o hidróxidos de menor solubilidad.
Caso Manganeso (Mn):
-
Convencionalmente precipita a pH ~11 como hidróxido (alto consumo químico y posterior neutralización).
-
Estrategia optimizada: elevar a pH 7–8 y oxidar con H₂O₂ → formación de óxidos de Mn y menor ajuste de pH, con ahorro en químicos y menos sales residuales.
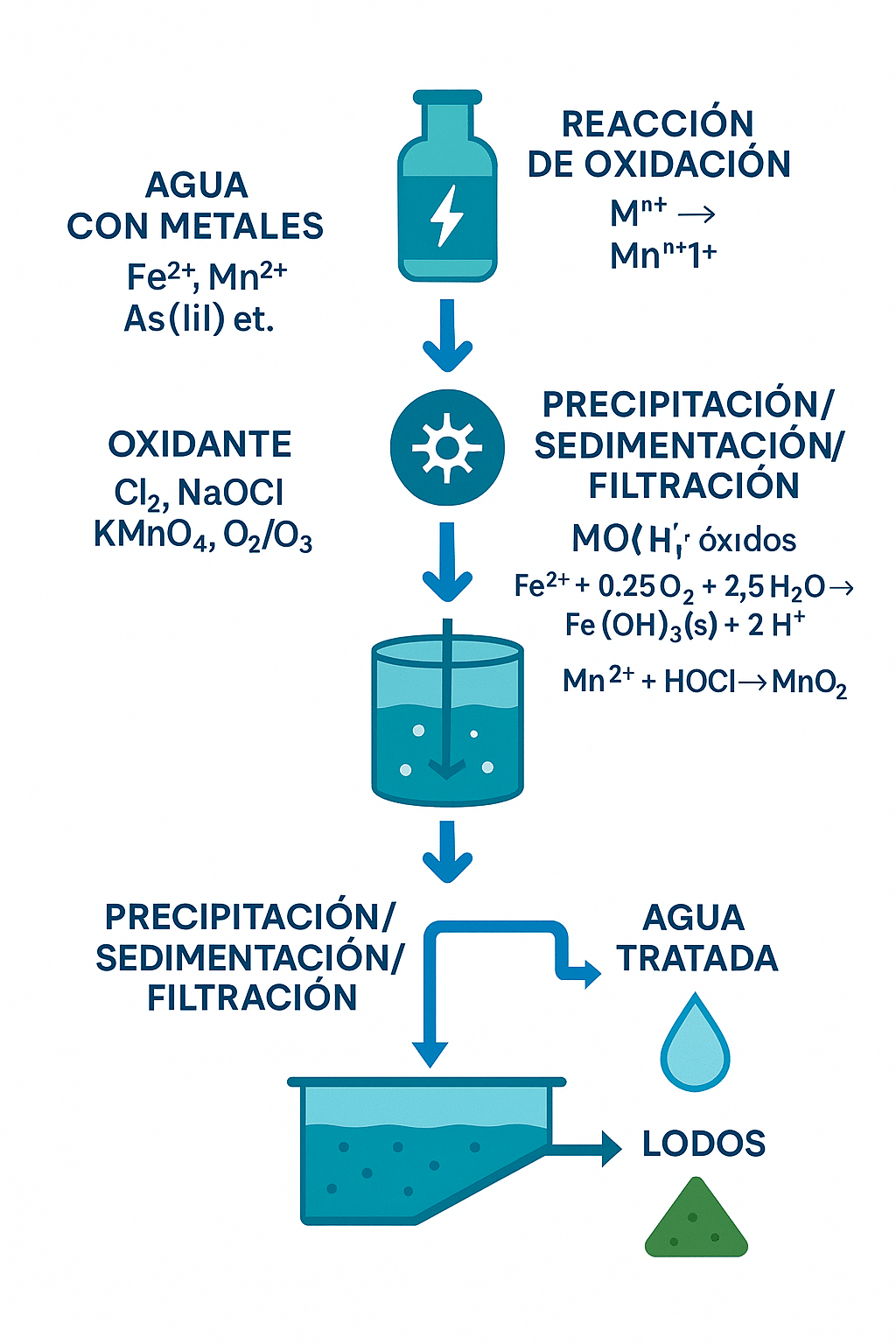
7) Arena verde (dióxido de manganeso) para Fe y Mn
La arena verde (medio con dióxido de manganeso) oxida y filtra Fe²⁺ → Fe³⁺ y Mn²⁺ → Mn⁴⁺.
-
Se regenera con hipoclorito o KMnO₄.
-
No sustituye al filtro de sólidos finos; su foco es hierro y manganeso disueltos.
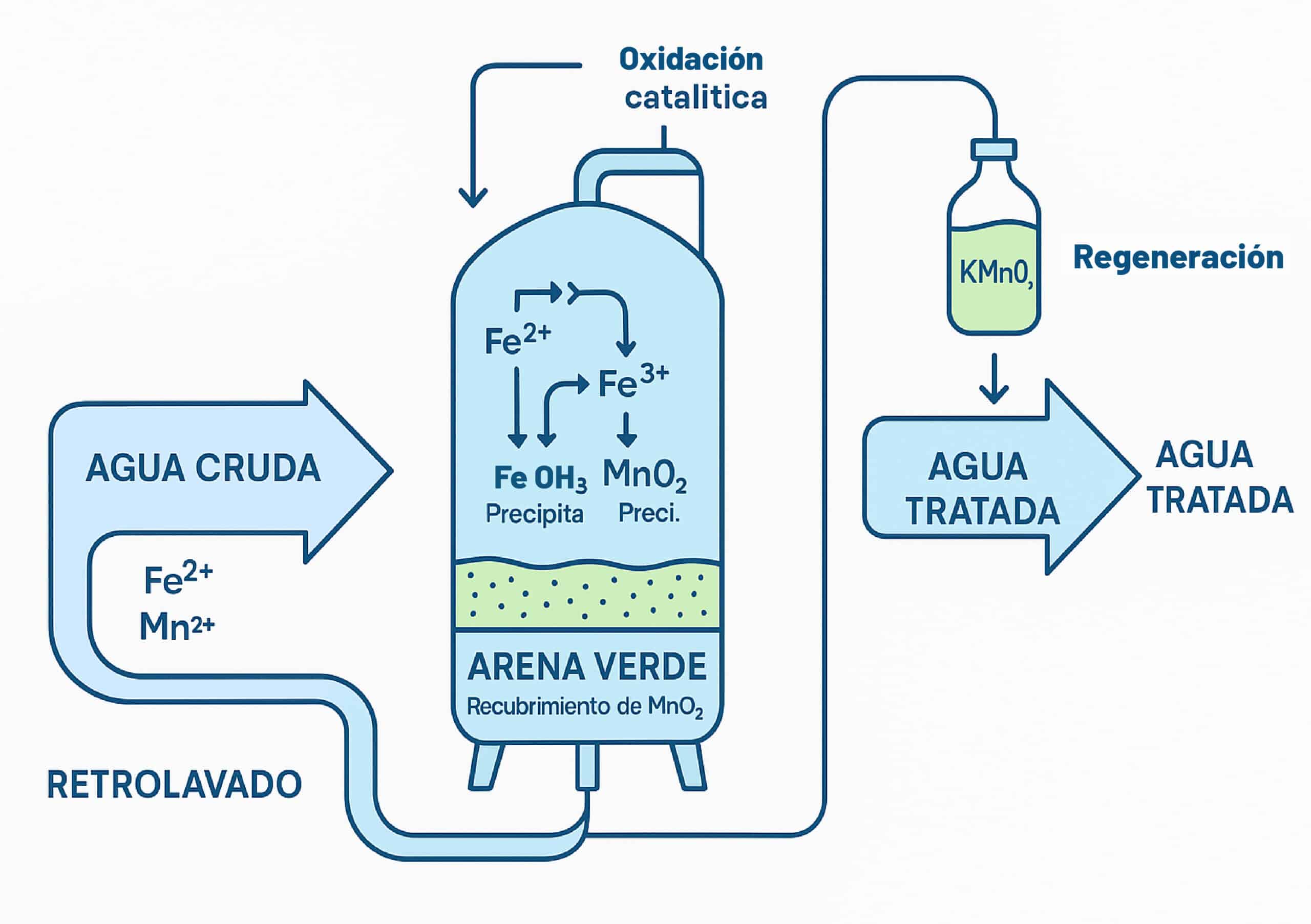
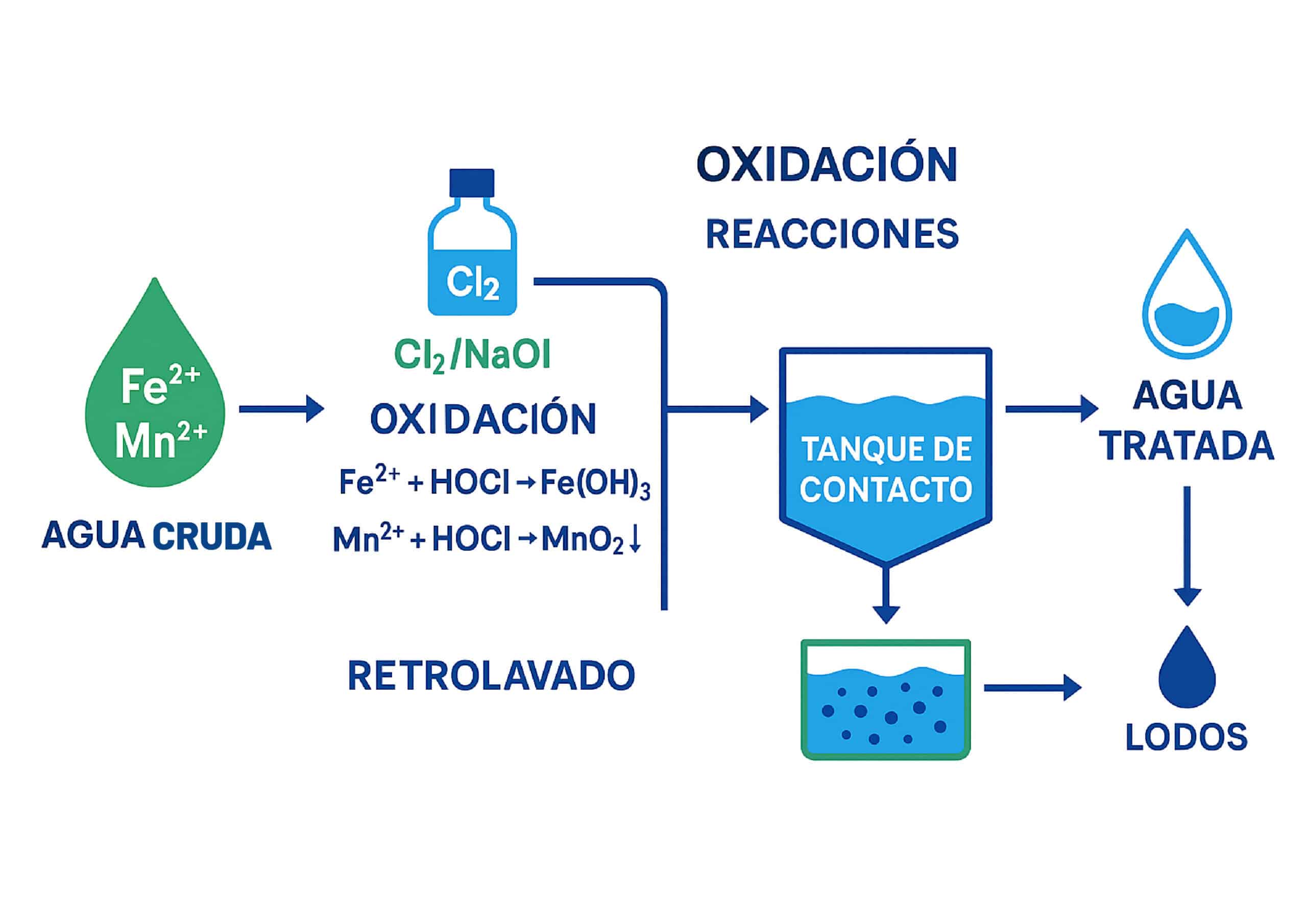
8) Eliminación de Fe y Mn con cloro
El cloro oxida: Fe²⁺ → Fe³⁺ y Mn²⁺ → Mn⁴⁺, formando hidróxidos/óxidos separables por filtración.
Requerimientos teóricos (referencia):
-
~3.2 mg/L de Cl₂ por 1 mg/L de Fe.
-
~1.9 mg/L de Cl₂ por 1 mg/L de Mn.
En la práctica, la dosis depende de amonio, materia orgánica y otros reductores: siempre validar con jar test y balance de cloro.
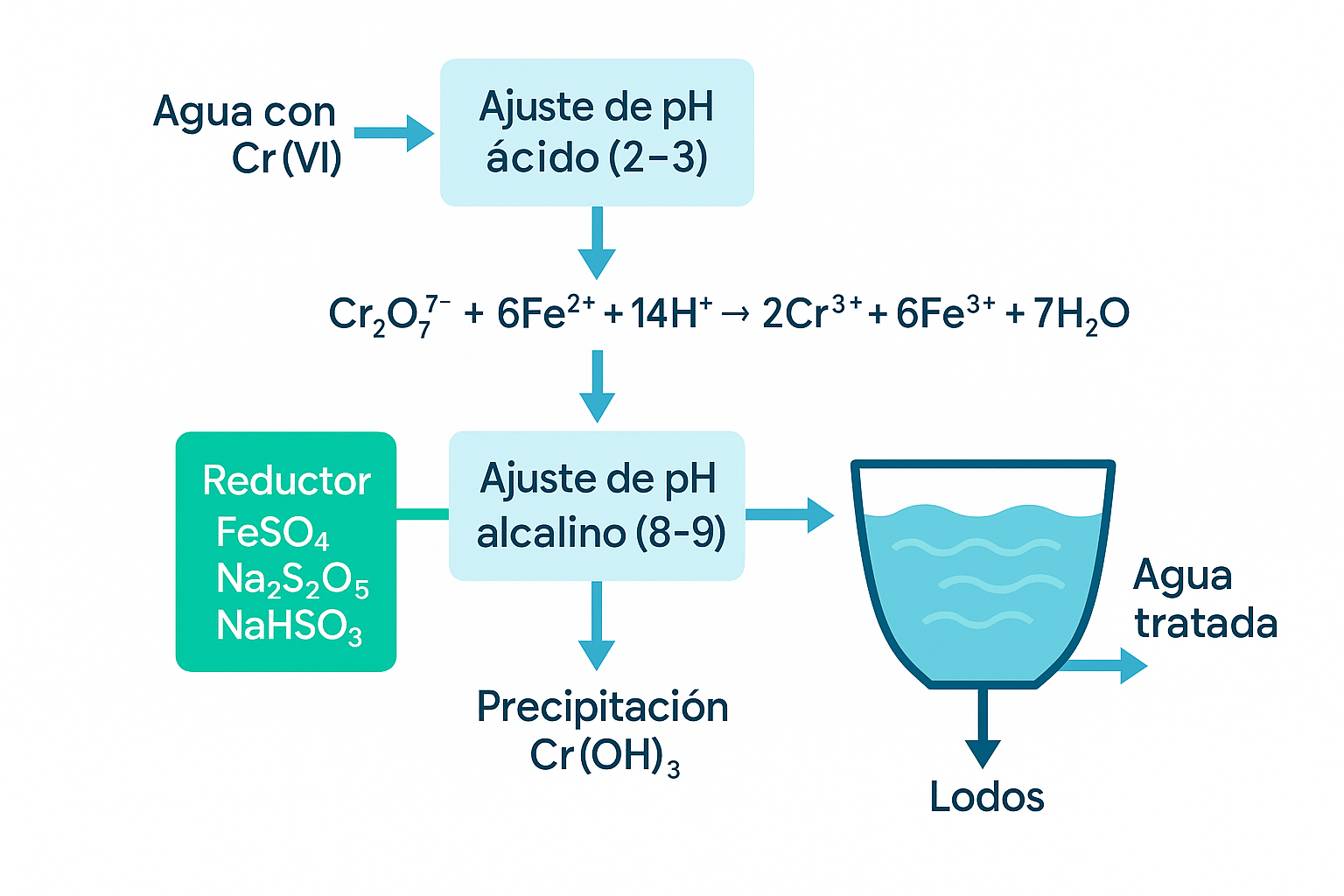
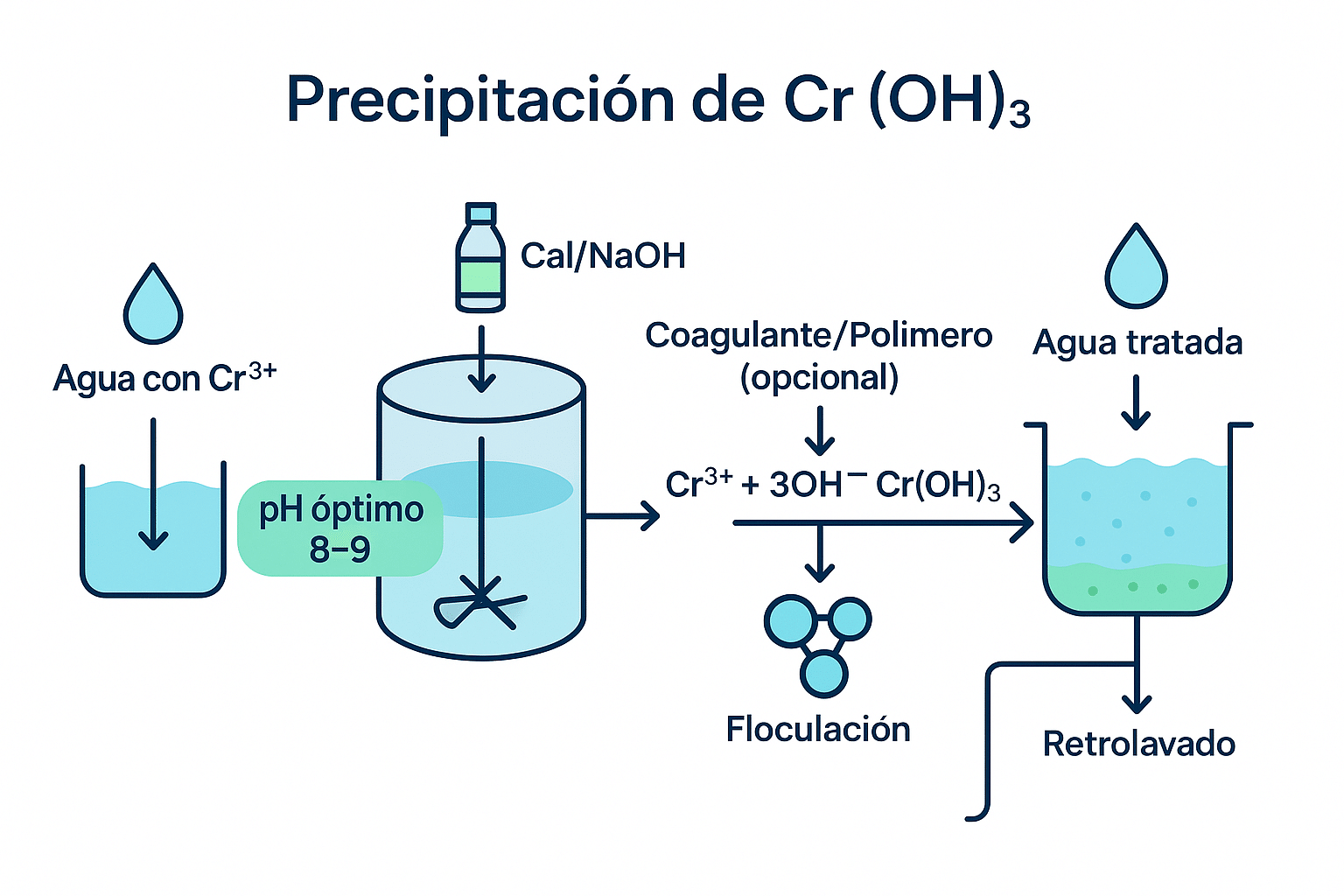
9) Cromo: Cr(VI) vs Cr(III)
-
Cr(III): precipita como Cr(OH)₃ elevando el pH (~8.5–9).
-
Cr(VI): no precipita con pH. Primero reducir (SO₂, metabisulfito, bisulfito) a Cr(III); luego elevar pH para Cr(OH)₃.
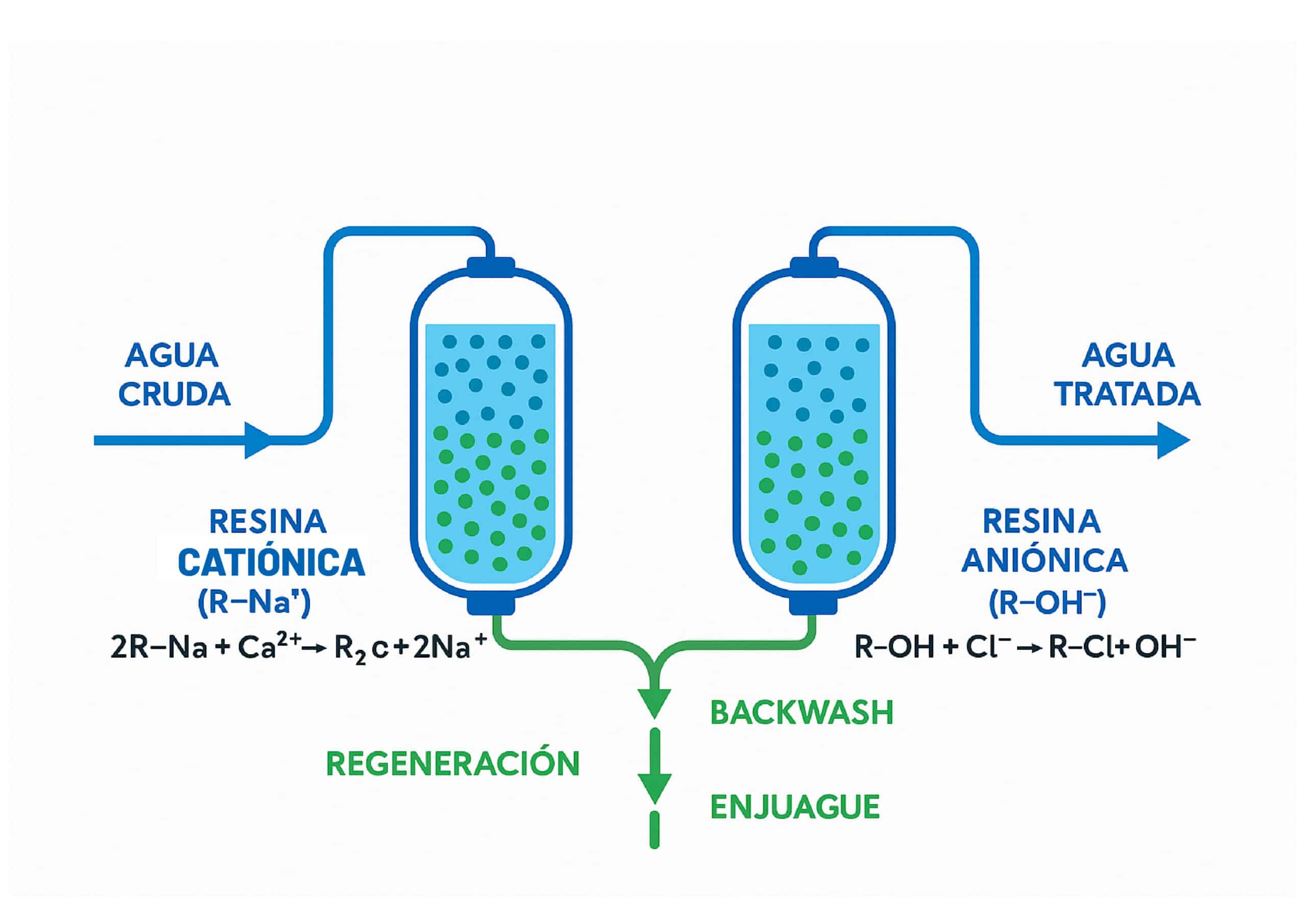
10) Intercambio iónico para metales específicos
Las resinas de intercambio iónico (catiónicas/aniónicas) capturan selectivamente iones metálicos.
-
Catiónicas: retienen Ag⁺, Pb²⁺, Cu²⁺, Ni²⁺, Zn²⁺, Fe²⁺/³⁺, etc.
-
Aniónicas: útiles cuando el metal está como complejo aniónico.
-
Regeneración: define costo operativo y gestión de regenerantes.
Ideal para:
-
Pulidos a bajas concentraciones.
-
Metales de alto valor (recuperación).
-
Cumplir LMP exigentes tras precipitación/filtración.
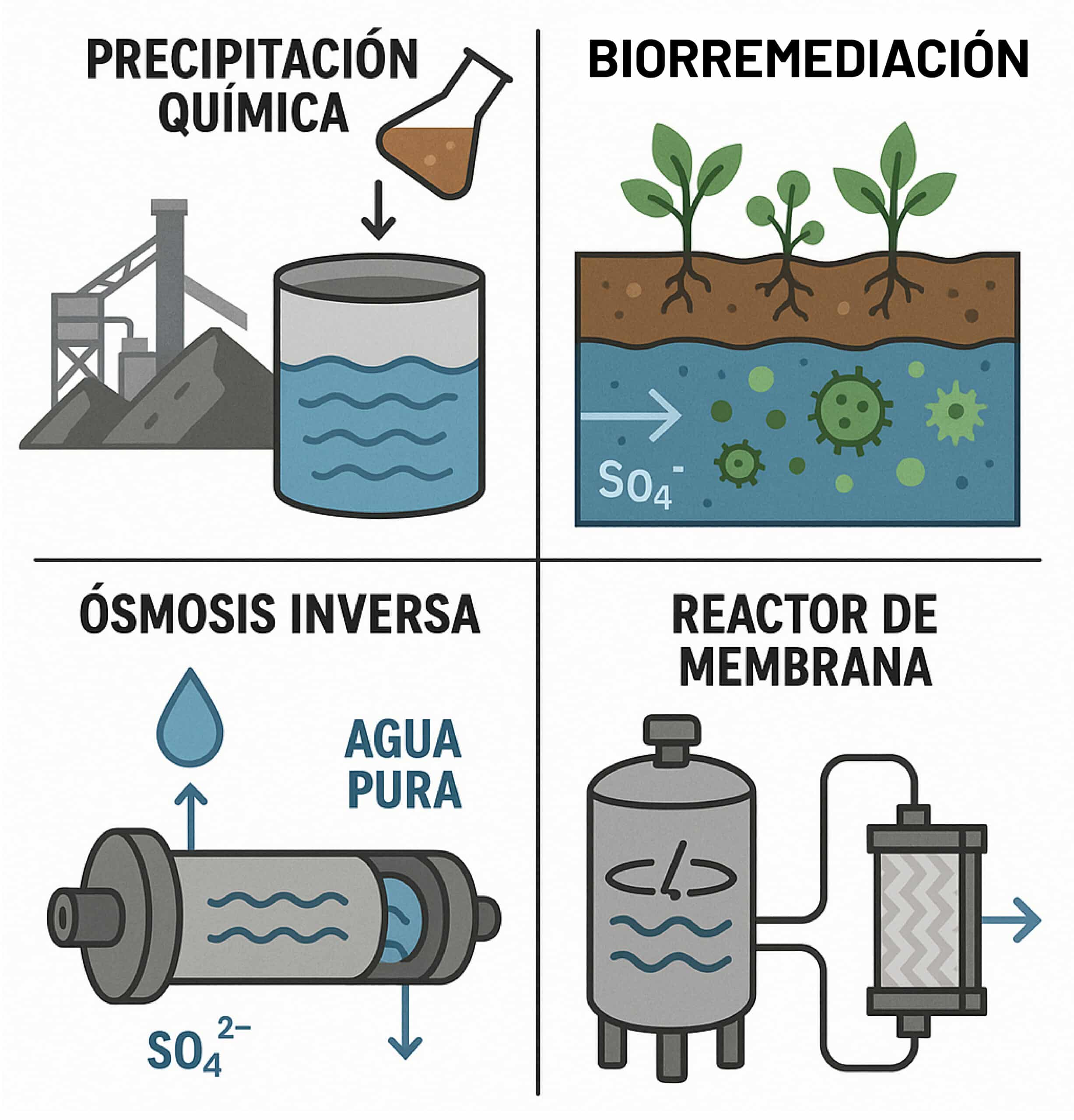
11) Sulfatos: el “duro de tratar”
Los sulfatos (SO₄²⁻) pueden limitar la descarga/reúso:
-
Con Ca(OH)₂, precipita CaSO₄ si se supera su solubilidad.
-
Alternativas: BaCl₂, Pb(NO₃)₂ (químicamente eficaces pero costosas y con riesgos), o combinaciones Al/Ca a pH > 10.5.
-
Evaluar CAPEX/OPEX y normativas por el manejo del residuo.
12) Criterios para seleccionar el tren de tratamiento
-
Caracterización completa del efluente (pH, ORP, metales disueltos y totales, sulfatos, cloruros, alcalinidad, TSS, DQO, temperatura).
-
Objetivo normativo (LMP/descarga/reúso).
-
Jar tests/pilotaje con escenarios pH/ORP y combinaciones (cal + oxidación, sulfuros, arena verde, intercambio iónico).
-
Gestión de lodos (volumen, % sólidos, disposición/valorización).
-
Seguridad (manejo de sulfuros, oxidantes, cloro; ventilación, EPP).
-
Integración OPEX (químicos, energía, recirculaciones, neutralizaciones) y automatización (control pH/ORP en línea).
13) Pros y contras resumidos
| Técnica | Pros | Contras | Uso típico |
|---|---|---|---|
| Cal (hidróxidos) | Robusta, económica | Muchos lodos, más sales | Abatimiento masivo |
| Sulfuros | Baja solubilidad, menos lodo | Manejo H₂S/ORP | Zn, Cu, Cd, Pb |
| Oxidación (H₂O₂/O₃/Cl₂) | Mejora remoción y cinética | Costo químico | Fe/Mn, refuerzo de hidrólisis |
| Arena verde | Compacta y selectiva | Requiere agua clara/regeneración | Fe/Mn disueltos |
| Intercambio iónico | Muy baja concentración final | Regenerantes/residuos | Pulido y metales valiosos |
La eliminación de metales pesados en efluentes mineros exige caracterización precisa, control de pH/ORP y pilotajes para definir la mejor combinación de procesos (precipitación, oxidación, sulfuros, filtración, intercambio iónico). Optimizar el sistema no solo garantiza cumplimiento normativo, sino que reduce lodos, químicos y costos a lo largo del ciclo de vida de la planta.
Flowen diseña e implementa trenes de tratamiento a medida para minería y metalurgia, con automatización pH/ORP, bajo OPEX y planes de operación y mantenimiento que aseguran desempeño estable.
📘 Referencia externa:
Consulta los Límites Máximos Permisibles (DS 010-2010-MINAM)